生物全合成的自组装纳米疫苗取得新进展
新型疫苗的快速研制对于防治突发传染病和重大疾病具有重要意义,而疫苗的组分设计、剂型构建、制备工艺与其应用效果和转化潜力密切相关。近日,过程工程所与军事医学研究院生物工程研究所合作,采用生物全合成技术构建了一种自组装蛋白纳米颗粒,以此为“底盘”制备的多糖和多肽类纳米疫苗,在多种动物模型中均展现出良好的安全性和高效的免疫应答水平,显著增强了传染病预防和肿瘤治疗的效果。相关工作发表于Advanced Materials(DOI:https://doi.org/10.1002/adma.202002940)。
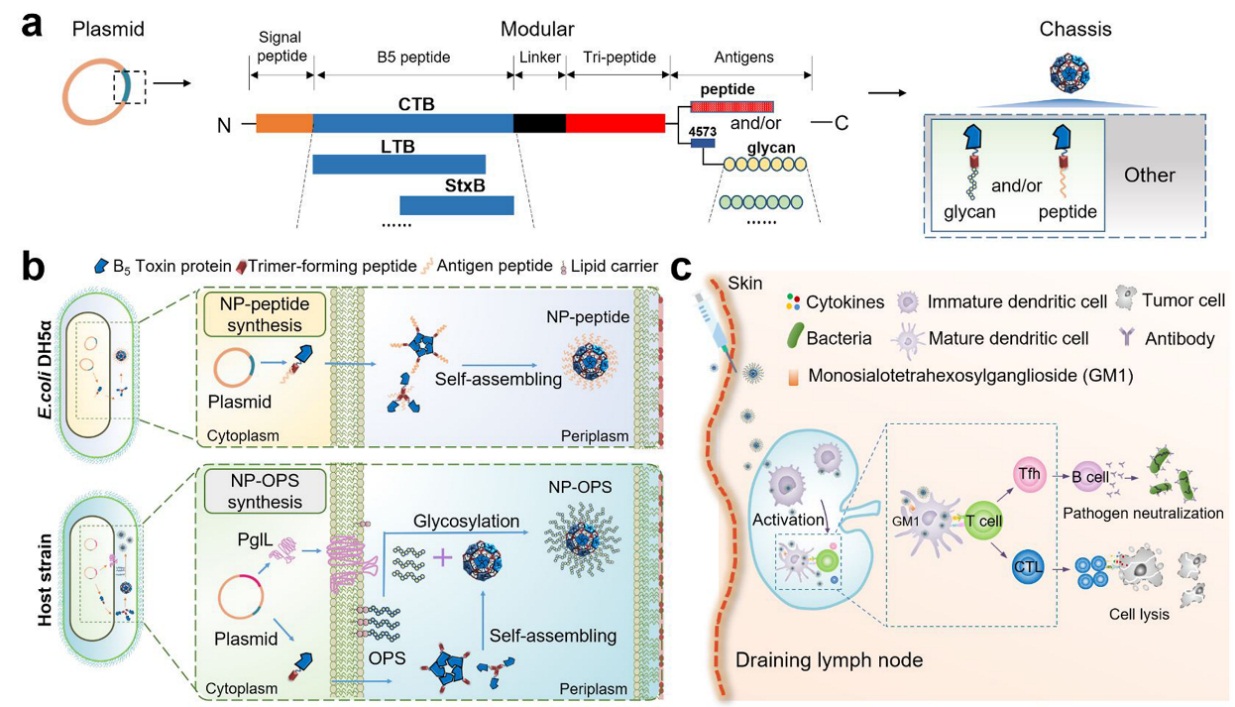
图 1 生物全合成纳米疫苗的制备及其免疫机制:(a)疫苗“底盘”的模块化设计及抗原组合示意图;(b)基于生物全合成的多肽及多糖结合疫苗的制备原理图;(c)纳米疫苗引发高效免疫应答的机制图。
针对现有纳米疫苗体系制备工艺繁琐、抗原负载量低、机体免疫应答较弱等难题,研究人员通过将细菌毒素B5(能够与细胞表面受体神经节苷脂结合)和非天然三聚体肽融合,构建了一种安全高效的自组装纳米疫苗“底盘”,用于新型疫苗的按需快速构建。
该纳米疫苗底盘为生物合成的蛋白骨架,避免了外源性合成材料的引入,保证了疫苗使用的安全性。同时,采用融合表达或蛋白糖基化修饰策略,可轻松实现多肽、多糖等不同类型抗原在“底盘”上的高效负载,无需额外化学偶联过程。另外,相比于单纯抗原,纳米疫苗避免了抗原在注射部位的快速清除,同时实现了淋巴结的有效富集。在无需额外添加佐剂的情况下,纳米疫苗能够快速激活抗原提呈细胞,并促进对抗原的摄取和交叉提呈,进而强化后续的免疫应答水平。
基于该纳米底盘构建的多糖结合疫苗在小鼠、猴等多种动物模型中成功诱导生成了针对志贺氏菌和甲型副伤寒沙门氏菌的高水平保护性抗体,其抗体滴度远优于商品化铝佐剂剂型。而基于该纳米底盘构建的肿瘤疫苗同样表现优异,能够快速激发小鼠体内的细胞免疫应答,显著抑制肿瘤生长并延长了小鼠存活时间。这种通用的“底盘”策略及模块化组合的疫苗设计理念,为抗肿瘤、抗细菌、抗病毒等高效疫苗的研发提供了新的思路。
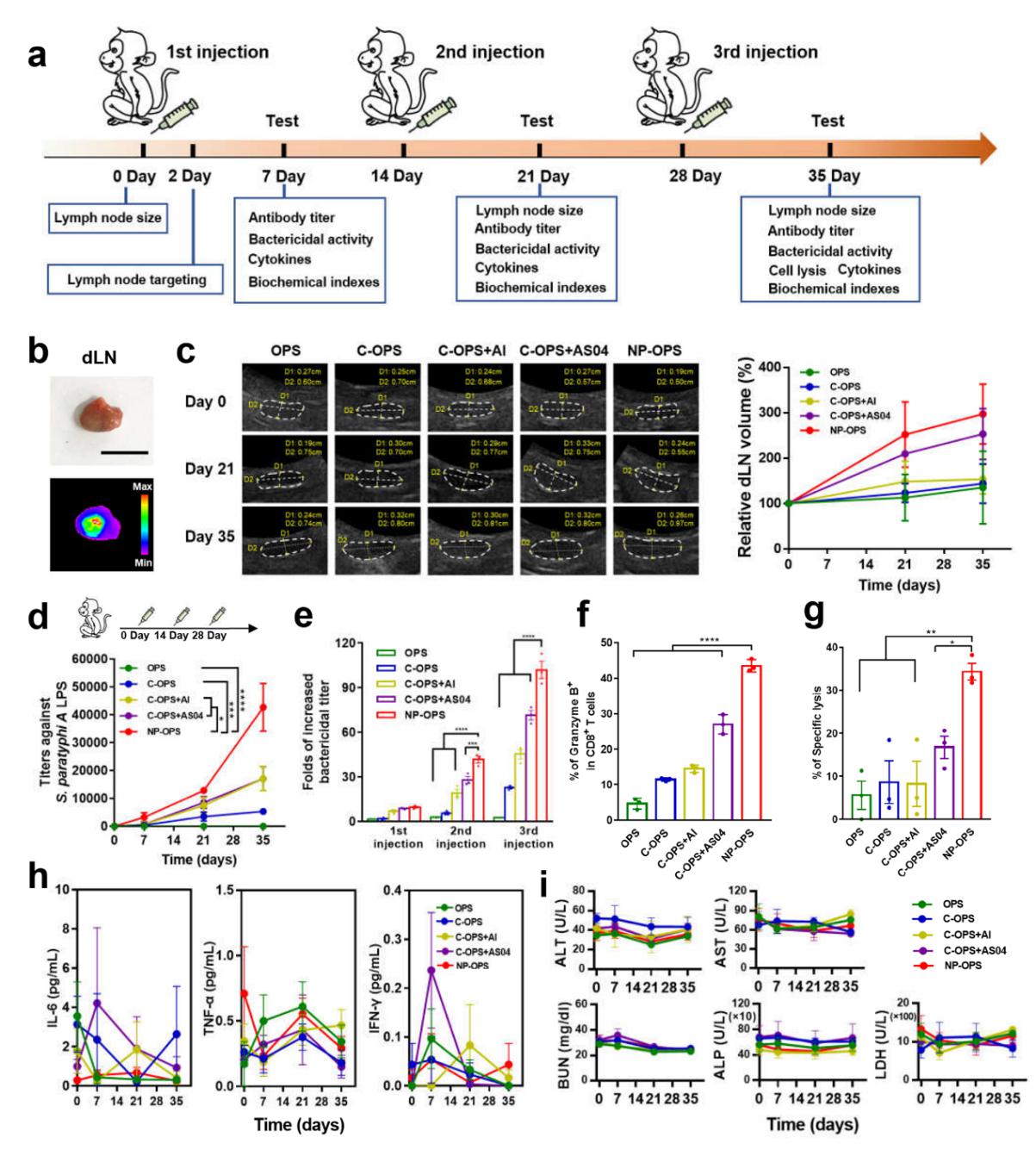
图 2 纳米疫苗在食蟹猴模型中的免疫效果评价。(a)纳米疫苗免疫效果评价流程图;(b)纳米疫苗的淋巴结靶向能力考察;(c)不同疫苗制剂免疫后的淋巴结大小;(d)不同疫苗制剂免疫后特异性抗体滴度水平;(e)抗体介导的血清杀菌能力;(f)血液中分泌颗粒酶B的CD8+ T细胞的百分比;(g)效应T细胞针对靶细胞的特异性杀伤能力;(h-i)纳米疫苗安全性评价。
自2006年起,过程工程所生化工程国家重点实验室生物剂型与生物材料团队的马光辉研究员和魏炜研究员对先进疫苗递送系统进行了率先探索和深入研究,发现和创制了一系列疫苗新剂型,解决了抗原免疫原性差、生物利用度低等难题,在肿瘤、乙肝、流感等重大疾病和传染病的预防和治疗研究中取得显著进展,相关工作相继发表于Nat Mater 2018, 17, 187、Nat Commun 2017, 8, 14537、Sci Adv 2020, 6, eaay7735、Adv Mater 2018, 31, 1801067、Adv Sci 2017, 4, 1700083、ACS Cent Sci 2019, 5, 796、Small 2018, 14, 1704272、Biomaterials 2015, 41, 1等期刊上,部分剂型已通过伦理批准进入临床前和临床研究。
军事医学研究院病原微生物生物安全国家重点实验室王恒樑研究员和朱力副研究员团队长期致力于病原微生物致病机制及其防控研究,特别是在细菌多糖结合疫苗的生物合成研究中取得显著进展,采用具有自主知识产权的细菌蛋白O-糖基化系统成功合成了针对志贺氏菌、甲型副伤寒沙门氏菌、布氏杆菌等新型疫苗,革新了传统的细菌多糖结合疫苗制备方法,相关工作相继发表于ACS Appl Mater Interfaces 2019, 11, 44933、mBio 2016, 7, e00443、npj Vaccines 2018, 3, 4、Microorganisms 2020, 8, 436等,已授权国内专利2项。
双方团队基于以往研究基础,利用生物合成和纳米组装相结合的策略,共同合作研发了该疫苗新剂型。潘超博士、吴军研究员和卿爽博士研究生为本论文的共同第一作者,王恒樑研究员、马光辉研究员、魏炜研究员和朱力副研究员为共同通讯作者。相关工作得到了国家自然科学基金群体项目/重点项目、国家科技重大专项、国家重点研发计划项目和中科院战略先导科技专项等支持。
(生物剂型与生物材料研究部)
