基于细菌的仿生肿瘤疫苗研究取得新进展
恶性肿瘤一直是困扰医学界的难题。近年来,肿瘤免疫疗法展现出良好的应用前景,被Science杂志评选为2013年度十大科学突破之首。其中,治疗性肿瘤疫苗通过激发自身免疫系统以达到清除或控制肿瘤生长的治疗方式是肿瘤免疫疗法的焦点。但肿瘤抗原的免疫原性较弱,使得现有治疗性肿瘤疫苗的使用效果仍不尽理想。因此,开发一种安全高效的治疗性肿瘤疫苗仍是一项极具挑战性和应用价值的研究课题。
自然界中病原微生物感染机体后能够引起强烈的免疫应答,其中的关键在于病原微生物的特殊形态及表面多重病原相关分子模式,能够促使病原体快速识别和捕获免疫细胞,引起机体强烈的免疫应答。受此启发,中科院过程工程研究所生化工程国家重点实验室生物剂型与生物材料课题组开发了一种具有多重仿病原体特征的新型仿生疫苗佐剂。通过对水热条件的优化,该疫苗制剂不但完整保留了细菌的形貌特点及病原体特征组分,同时还具备了中空多孔的结构,极大地促进了抗原及其他免疫刺激剂的装载(图1)。研究结果表明,该仿生菌体能够快速地被免疫系统识别、捕获并进行抗原呈递,进而引起强烈的细胞免疫应答(图2)。动物实验进一步证明,该仿生疫苗制剂在多种肿瘤模型中均具有良好的抑瘤效果和抗肿瘤转移能力(图3)。该研究创新性地提出以病原微生物本身为对象的仿生设计理念,为今后治疗性疫苗的研发提供了全新的设计思路。
相关研究发表在Advanced Science(2017,1700083)上,倪德志博士和博士生卿爽为本文的并列第一作者,中科院过程所马光辉研究员、魏炜研究员为通讯作者。该研究得到了国家科技重大专项(2014ZX09102045-004)、973项目(2013CB531500)、国家自然科学基金(21622608)等支持。
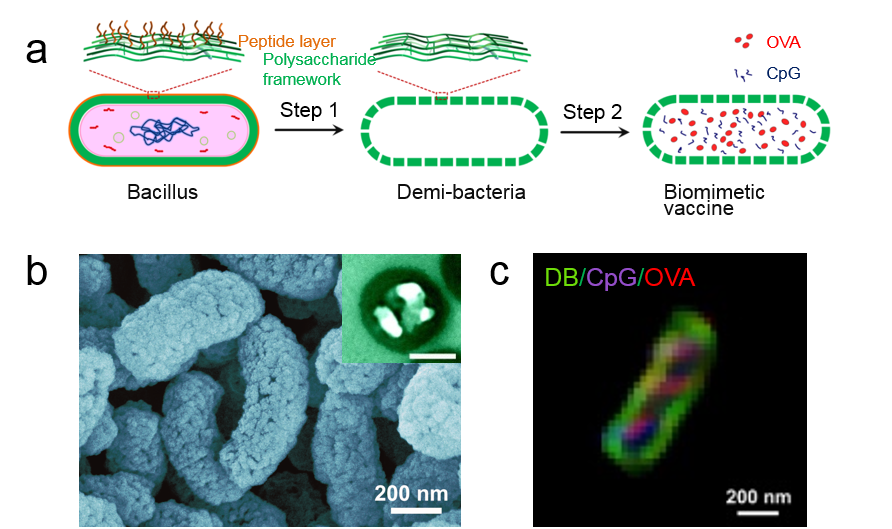
图 1 仿生疫苗制备:a) 仿生疫苗构建示意图;b) 中空多孔DB的SEM照片;c) DB装载CpG和OVA的超分辨共聚焦照片。

图 2 DB与免疫细胞的相互作用:a)DB被树突状细胞内吞后的共聚焦照片;b)DB刺激后树突状细胞表面共刺激因子与特异性MHC分子表达;c)免疫接种后小鼠体内特异性CD8+ T细胞的增殖情况。
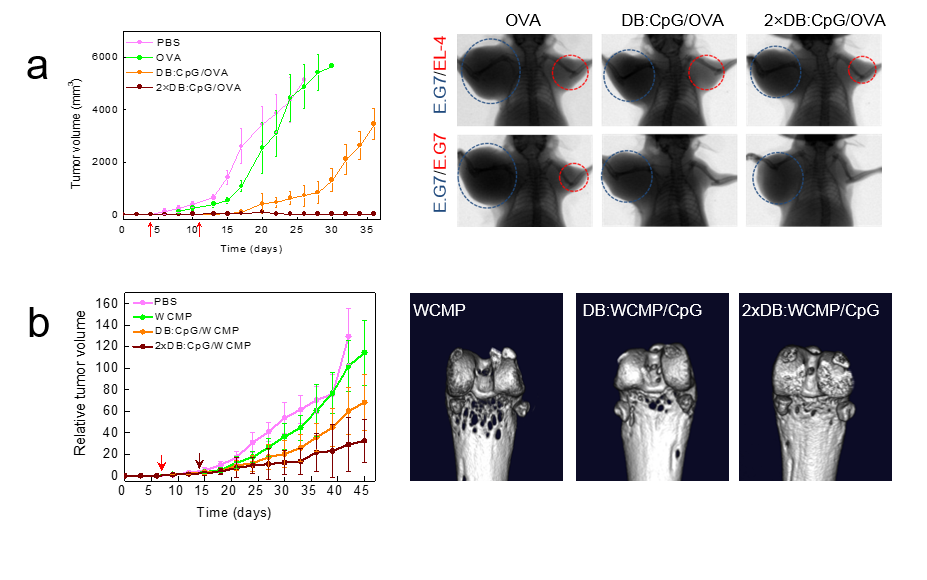
图 3 仿生疫苗抑瘤效果与抗肿瘤转移能力显著:a) E.G7肿瘤模型的抑瘤曲线与代表性肿瘤转移灶照片;b) 4T1肿瘤模型的抑瘤曲线及骨转移情况。
(生物剂型与生物材料研究部)
